Caratteristiche
Caratteristica: predisposizione alle infezioni da peste e autoimmunità (ERAP2)
Dott. Haran Sivapalan
/
28 novembre 2022

Che cos'è la presentazione dell'antigene?
Ti sei mai chiesto come fa il nostro sistema immunitario a «sapere» quali cellule attaccare?
I batteri, i virus, i funghi e altri microrganismi nocivi (noti collettivamente come agenti patogeni) presentano marcatori molecolari specifici che li identificano come «estranei» o «non propri». Questi marcatori, che comprendono i componenti della parete cellulare dei batteri, le proteine che costituiscono il flagello (la struttura simile a una coda che permette il movimento) dei protozoi o l'involucro proteico di un virus, sono chiamati antigeni.
Riconoscendo e “memorizzando” antigeni specifici, il nostro sistema immunitario è in grado di attivare una risposta adeguata nei confronti di determinati agenti patogeni e di individuarli rapidamente la volta successiva che entrano nell’organismo. Questo è il principio alla base dell’immunità adattativa e spiega perché le vaccinazioni contribuiscono a proteggerci dalle malattie.

Un tipo di globuli bianchi (linfociti), noti come cellule B, possiede recettori antigenici specializzati, chiamati recettori delle cellule B (BCR), che si legano agli antigeni integrali presenti nei batteri e in altri organismi. Quando ciò accade, le cellule B si attivano, si moltiplicano e iniziano a produrre anticorpi diretti contro l'antigene specifico, contribuendo a neutralizzare l'organismo invasore. Questo processo è illustrato nell'immagine qui sopra.
Esiste anche un altro tipo di globulo bianco, noto come cellula T. Anziché produrre anticorpi, le cellule T contribuiscono a distruggere le cellule infette e aiutano a coordinare una risposta immunitaria più ampia contro un agente patogeno.

Esistono due tipi di cellule T:
- Cellule T citotossiche (note anche come cellule T CD8+) – che distruggono le cellule infettate da agenti patogeni.
- Le cellule T helper (note anche come cellule T CD4+) secernono molecole di segnalazione (citochine) che attivano altre cellule immunitarie e contribuiscono a coordinare una risposta immunitaria più ampia. Le cellule T helper sono così chiamate perché aiutano le cellule B a produrre anticorpi e le cellule T citotossiche a distruggere le cellule infette.
Le cellule T possiedono anch'esse dei recettori antigenici, chiamati recettori delle cellule T (TCR), in grado di riconoscere gli antigeni specifici presenti sui batteri e simili. A differenza di quelli delle cellule B, i recettori antigenici delle cellule T non sono in grado di legarsi agli antigeni nella loro interezza.
Al contrario, gli antigeni (ad esempio una proteina presente sulla superficie di un batterio) devono prima essere scomposti in frammenti più piccoli, prima di essere presentati alle cellule T affinché queste possano orchestrare una risposta immunitaria mirata.
Questo processo di frammentazione, elaborazione e presentazione degli antigeni alle cellule T è noto come presentazione dell'antigene.
- Nozioni di base sulla presentazione dell'antigene
Quando le nostre cellule vengono infettate, ad esempio, da un batterio, frammentano l’antigene batterico in parti più piccole (chiamate peptidi antigenici) utilizzando enzimi specializzati. Questi peptidi antigenici più piccoli, che sono ancora in grado di identificare in modo univoco il batterio, vengono poi combinati con una proteina delle nostre cellule chiamata MHC (Complesso Maggiore di Istocompatibilità).
Il peptide antigenico batterico e la proteina MHC vengono quindi presentati insieme sulla superficie della cellula infetta, come una sorta di codice a barre immunologico. Le cellule T possono quindi “scansionare” questo codice a barre utilizzando il loro recettore delle cellule T. Ciò consente alle cellule T di riconoscere altre cellule infette, in modo che possano essere distrutte o lisate direttamente o indirettamente (rispettivamente dalle cellule T citotossiche e dalle cellule T helper).

Fonte: Introduzione alla risposta immunitaria. Manuale introduttivo alla risposta immunitaria. 2014:3–20. doi: 10.1016/B978-0-12-385245-8.00001-7. Pubblicazione elettronica: 10 ottobre 2014. PMCID: PMC7184560.
Esistono due classi di proteine MHC che le nostre cellule utilizzano per presentare gli antigeni; la scelta dipende dal modo in cui la cellula viene infettata e dal fatto che l'antigene (o, più precisamente, il peptide antigenico) venga presentato a una cellula T citotossica o a una cellula T helper.
- L'MHC di classe I viene utilizzato per batteri, virus e altri agenti patogeni che hanno invaso le cellule (agenti patogeni intracellulari). Serve a presentare i peptidi antigenici di questi agenti patogeni intracellulari ai linfociti T citotossici. Praticamente tutte le nostre cellule sono in grado di produrre MHC di classe I, quindi qualsiasi cellula che sia stata infettata da un agente patogeno può essere presa di mira e distrutta dai linfociti T citotossici. Anche le cellule immunitarie come i macrofagi possono fagocitare le cellule infette e presentare gli antigeni utilizzando l'MHC di classe I ai linfociti T citotossici.
- L'MHC di classe II viene utilizzato sia per i patogeni intracellulari che per quelli extracellulari. Serve a presentare i peptidi antigenici alle cellule T helper. I patogeni extracellulari potrebbero dover essere fagocitati da cellule immunitarie specializzate (come le cellule dendritiche (DC) o i macrofagi), prima che il loro antigene possa essere presentato alle cellule T helper. Solo alcuni tipi di cellule immunitarie (note collettivamente come cellule presentanti l'antigene) producono l'MHC di classe II. MHC di classe I
Se desiderate approfondire l'argomento delle varie cellule del sistema immunitario, della presentazione dell'antigene e di come si acquisisce l'immunità, questa guida introduttiva della "Elsevier Public Health Emergency Collection" è un ottimo articolo.
Che cos'è l'ERAP2?
L'ERAP2 (aminopeptidasi 2 del reticolo endoplasmatico) è un enzima coinvolto nella nostra risposta immunitaria alle infezioni.
Più precisamente, l'ERAP2 è coinvolto nella presentazione ai linfociti T degli antigeni provenienti dai patogeni che hanno infettato le cellule, facilitando la distruzione immunitaria di queste cellule infette.
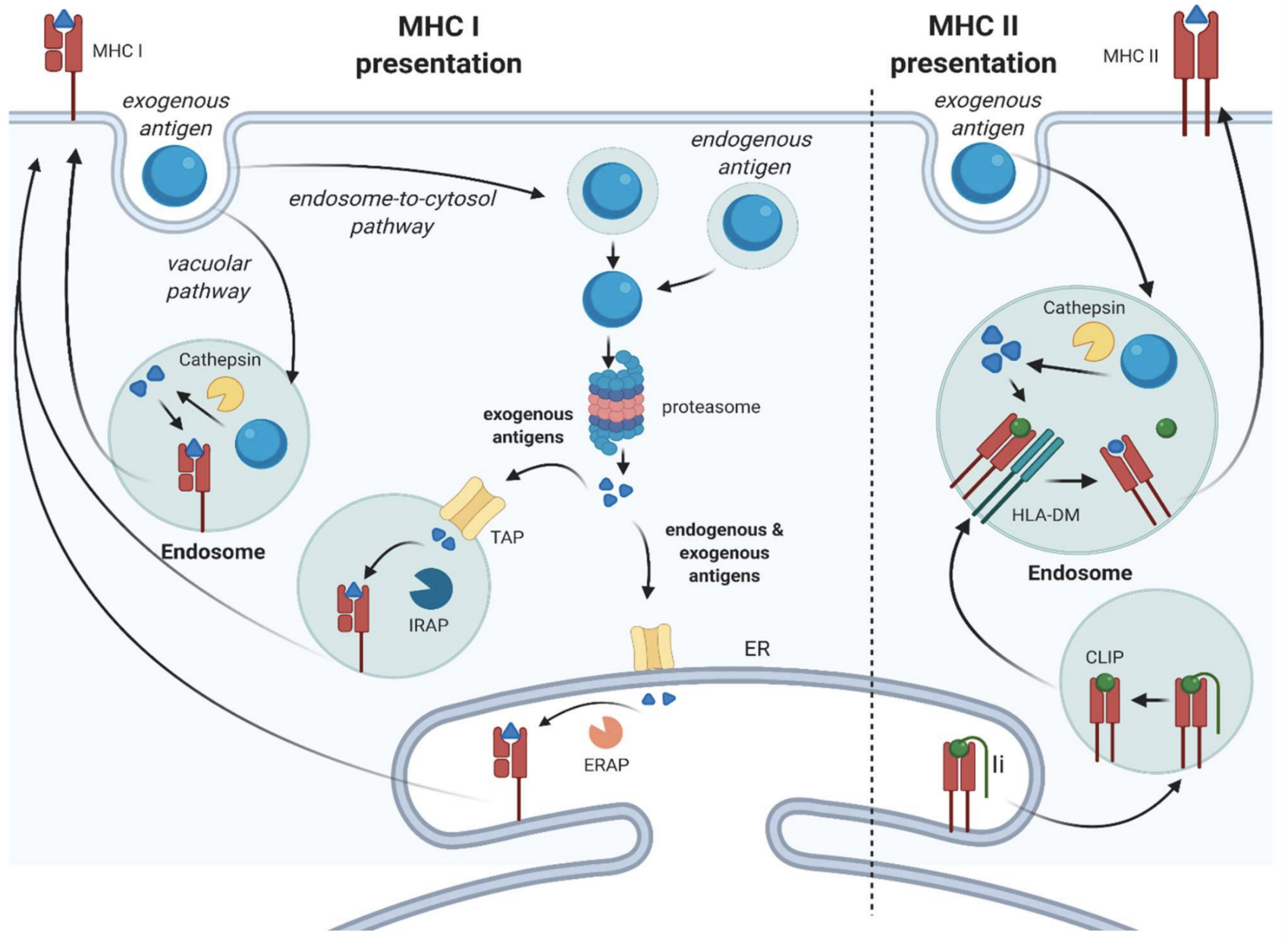
Fonte: Harryvan, T. J., de Lange, S., Hawinkels, L. J. A. C., & Verdegaal, E. M. E. (2021). L'ABC della presentazione dell'antigene da parte delle cellule stromali non professionali presentanti l'antigene. International Journal of Molecular Sciences, 23(1), 137. MDPI AG. Estratto da http://dx.doi.org/10.3390/ijms23010137
Come spiegato nella sezione precedente, gli antigeni provenienti da batteri, virus e altri agenti patogeni devono essere frammentati in peptidi antigenici più piccoli e quindi legati alle proteine MHC prima di poter essere presentati alle cellule T.
L'enzima ERAP2, in particolare, è coinvolto nella rifinitura finale dei peptidi antigenici prima che questi vengano caricati sulla proteina MHC di classe I.
Il complesso risultante, costituito dalla proteina MHC di classe I e dal peptide antigenico, può quindi essere presentato alle cellule T citotossiche. Ciò consente alle cellule T citotossiche di riconoscere e distruggere altre cellule infettate dallo stesso agente patogeno, poiché anche tali cellule infette esprimeranno lo stesso peptide antigenico.
L'enzima ERAP2 è codificato dal gene ERAP2.
In che modo le varianti del gene ERAP2 influenzano la risposta immunitaria alle infezioni?
Un SNP (polimorfismo a singolo nucleotide) nel gene ERAP2, denominato rs2549794, dà origine a due diverse varianti o alleli del gene ERAP2:
- la variante «C»
- la variante «T».
Alcuni studi hanno dimostrato che la variante «C» è associata a un’espressione di ERAP2 cinque volte superiore rispetto alla variante «T». Ad esempio, in uno studio sono state analizzate le cellule immunitarie di soggetti privi della variante «C», o in possesso di una o due copie della stessa (genotipi TT, CT e CC, rispettivamente), al fine di valutare le differenze nell’espressione del gene ERAP2. (L'espressione genica è essenzialmente il processo mediante il quale le istruzioni contenute in un gene vengono lette e utilizzate per produrre la proteina codificata. In linea di massima, si può affermare che una maggiore espressione del gene ERAP2 comporta una maggiore produzione dell'enzima ERAP2 da parte di varie cellule).
I ricercatori hanno esaminato sia i livelli di base dell'espressione genica (in condizioni di non stimolazione/non infezione), sia l'espressione genica quando le cellule sono state incubate con la Yersinia pestis, il batterio responsabile della peste.
Come illustrato nei grafici riportati di seguito, le cellule immunitarie delle persone con una o due copie della variante C (genotipi CT e CC) hanno mostrato un’espressione di ERAP2 significativamente più elevata rispetto a quelle delle persone con genotipo TT. Ciò è risultato vero sia quando le cellule immunitarie erano non stimolate/non infette, sia in presenza di un’infezione da Y. pestis.


Fonte: Klunk, J., Vilgalys, T. P., Demeure, C. E., Cheng, X., Shiratori, M., Madej, J., ... & Barreiro, L. B. (2022). L'evoluzione dei geni immunitari è associata alla peste nera. Nature, 1-8.
Lo stesso studio ha inoltre sottoposto i globuli bianchi (macrofagi) a incubazione con il batterio Yersinia pestis per verificare la loro efficacia nell'uccidere i batteri e nell'impedirne la replicazione.
Come mostrano i grafici a scatola riportati di seguito, i globuli bianchi prelevati dai soggetti con genotipo CC hanno eliminato la percentuale maggiore di batteri, seguiti dal genotipo CT e infine dal genotipo TT.

Fonte: Klunk, J., Vilgalys, T. P., Demeure, C. E., Cheng, X., Shiratori, M., Madej, J., ... & Barreiro, L. B. (2022). L'evoluzione dei geni immunitari è associata alla peste nera. Nature, 1-8.
Nel complesso, questi risultati suggeriscono che , aumentando l'espressione del gene ERAP2, la variante «C» (rs2549794) favorisce una risposta immunitaria più efficace nei confronti di vari agenti patogeni, tra cui il batterio Yersinia pestis .
Più precisamente, si ritiene che una maggiore espressione di ERAP2 associata alla variante «C» consenta una presentazione più efficace degli antigeni batterici alle cellule T citotossiche (cellule CD8+). Ciò potrebbe consentire alle cellule T citotossiche di distruggere più facilmente le cellule infette, contribuendo a debellare più rapidamente le infezioni batteriche.
Cos'è la peste?
La peste è una malattia infettiva causata dalla Yersinia pestis , che si trova tipicamente nei piccoli mammiferi (in particolare nei roditori) e nelle loro pulci.
L'infezione da batteri avviene quando una persona viene morsa da una pulce infetta. Il batterio può diffondersi anche attraverso il contatto non protetto con fluidi corporei infettivi o materiali contaminati (ad esempio, maneggiando tessuti animali infetti), oppure inalandone le goccioline respiratorie emesse da una persona infetta (nel caso della peste polmonare).

Immagine di bubboni pestiferi all'inguine. Fonte: Wikimedia Commons
I sintomi generali della peste comprendono febbre, mal di testa, brividi e spossatezza, mentre i sintomi più specifici variano a seconda del tipo di peste e della via di contagio. A questo proposito, esistono tre forme principali di peste:
- Peste bubbonica: la forma più comune di peste, causata dal morso di una pulce infetta. I batteri presenti nel morso della pulce raggiungono i linfonodi vicini, provocandone il gonfiore, il dolore e l'infiammazione. Questi linfonodi ingrossati sono noti come «buboni».
- Peste polmonare: questa forma di peste colpisce i polmoni ed è causata dall'inalazione delle goccioline respiratorie emesse da altre persone affette da peste polmonare. Anche la peste bubbonica, se non curata e se si diffonde ai polmoni, può causare la peste polmonare.
- Peste setticemica: si verifica quando l'infezione da peste si diffonde nel flusso sanguigno. Può causare emorragie e portare allo shock settico.
Nel corso della storia, diverse pandemie di peste hanno causato la morte di milioni di persone in tutto il mondo. La pandemia forse più tristemente nota è stata la peste nera: quella che tra il 1346 e il 1350 d.C. colpì l’Europa, il Medio Oriente e il Nord Africa, riducendo la popolazione del 30-50%.
La peste continua a colpire le persone ancora oggi, con focolai in diversi paesi dell’Africa, del Nord America, del Sud America e dell’Asia. A livello mondiale, tra il 2010 e il 2015 sono stati segnalati 3.248 casi di peste. A partire dagli anni ’90, la maggior parte dei casi si è verificata in Africa, con il Madagascar che registra l’incidenza più elevata.
Fortunatamente, la peste può essere trattata e curata efficacemente con antibiotici comuni. Se non viene curata, tuttavia, la peste polmonare può diventare rapidamente mortale.
Per ulteriori informazioni sulla peste, le pagine del CDC (Centri per il controllo e la prevenzione delle malattie) e dell'OMS (Organizzazione mondiale della sanità) rappresentano ottime fonti di informazione.
In che modo le varianti del gene ERAP2 hanno influito sulla suscettibilità alla peste nera?
Uno studio recente suggerisce che la variante «C» (rs2549794) del gene ERAP2 offra una maggiore protezione contro l'infezione da Yersinia pestis e la peste; storicamente, infatti, i portatori della variante «C» hanno avuto maggiori probabilità di sopravvivere alla pandemia di peste nota come «Morte Nera» (1346-1350 d.C.).
Lo studio ha datato e analizzato campioni di DNA di persone sepolte in vari cimiteri di Londra e in tutta la Danimarca. Questi individui erano morti prima (850-1250 d.C.), durante (1348-1349) o dopo (1350-1800 d.C.) la peste nera.
Secondo la teoria evoluzionistica della selezione naturale, se una variante genetica aumenta le probabilità di sopravvivenza, ci si aspetterebbe che tale variante venga selezionata e che, di conseguenza, la sua frequenza nella popolazione aumenti nel corso delle generazioni. Su questa base, se una variante genetica favorisce la sopravvivenza durante una pandemia di peste, ci si aspetterebbe che questa variante benefica fosse più diffusa negli individui deceduti dopo la peste nera rispetto a quelli deceduti prima e durante la peste nera.
Al contrario, se una particolare variante genetica rendesse qualcuno più vulnerabile alla peste, ci aspetteremmo che la frequenza di tale variante nelle popolazioni fosse significativamente inferiore dopo la peste nera. Questo perché le persone portatrici di questa variante sfavorevole avrebbero avuto meno probabilità di sopravvivere alla peste nera e di trasmettere i propri geni alle generazioni future.

Fonte: Klunk, J., Vilgalys, T. P., Demeure, C. E., Cheng, X., Shiratori, M., Madej, J., ... & Barreiro, L. B. (2022). L'evoluzione dei geni immunitari è associata alla peste nera. Nature, 1-8.
Come illustrato nel grafico sopra, è emerso che la frequenza della variante «C» del gene ERAP2 era significativamente più elevata nelle persone decedute dopo la peste nera rispetto a quelle decedute prima e durante la peste nera. (I marcatori blu indicano i campioni di DNA provenienti dalla Danimarca; quelli rossi indicano i campioni provenienti dai siti funerari di Londra).
Ciò suggerisce fortemente che la variante «C» avesse un effetto protettivo contro l’infezione da Yersinia pestis e aumentasse le probabilità di sopravvivenza durante la pandemia della peste nera. Infatti, i ricercatori hanno calcolato che le persone in possesso di due copie della variante «C» (ovvero quelle con genotipo CC) avevano circa il 40% di probabilità in più di sopravvivere alla peste nera rispetto a quelle che ne erano prive (ovvero quelle con genotipo TT).
Il vantaggio in termini di sopravvivenza della variante «C» è probabilmente dovuto ai suoi effetti sull'espressione di ERAP2 (come spiegato in precedenza). I portatori della variante «C» con un'espressione più elevata di ERAP2 potrebbero essere stati maggiormente in grado di presentare gli antigeni del batterio Yersinia pestis alle cellule T citotossiche. Ciò favorirebbe una risposta immunitaria più forte e una distruzione più efficace delle cellule infettate dal batterio.
In che modo le varianti del gene ERAP2 influenzano la suscettibilità ad altre infezioni?
Uno studio preliminare pubblicato di recente ha associato la variante «T» (rs2549794) del gene ERAP2 a una maggiore predisposizione alle infezioni respiratorie, come la polmonite.
Lo studio ha raccolto i dati provenienti da tre ampie coorti di studio (UK Biobank, FinnGen e GenoMICC) e ha esaminato i genotipi del gene ERAP2 nei soggetti (casi) ricoverati in ospedale per polmonite, COVID-19 grave e sepsi. La frequenza dei genotipi del gene ERAP2 è stata poi confrontata con quella dei soggetti di controllo sani.
Se una particolare variante del gene ERAP2 aumentasse la suscettibilità alle infezioni respiratorie, ci aspetteremmo che tale variante fosse più frequente nei casi rispetto ai controlli. Per i portatori di questa variante di rischio, la probabilità di essere un caso piuttosto che un controllo sano sarebbe maggiore rispetto ai non portatori.

Fonte: Hamilton, F. W., Mentzer, A. J., Parks, T., Baillie, J. K., Smith, G. D., Ghazal, P. e Timpson, N. J. (2022). Le variazioni del gene ERAP2 hanno effetti opposti sulle infezioni respiratorie gravi e sulle malattie autoimmuni. medRxiv.
Come si evince dalla tabella sopra riportata, la variante «T», rispetto alla variante «C», era associata a un aumento del 2,5% del rischio di polmonite, a un aumento del 7,8% del rischio di ricovero in terapia intensiva per polmonite e a un aumento del 2,7% del rischio di COVID-19 grave. La variante «T» non sembrava tuttavia aumentare il rischio di sepsi.
Gli autori dello studio hanno ipotizzato che l'espressione relativamente più bassa di ERAP2 causata dalla variante «T» comporti una presentazione meno efficace degli antigeni batterici e virali ai linfociti T citotossici e una risposta infiammatoria delle citochine più debole. Ciò contribuirebbe a una risposta immunitaria meno efficace nei confronti di determinati agenti patogeni, rendendo i portatori della variante «T» più suscettibili alle infezioni respiratorie.
In che modo le varianti del gene ERAP2 influenzano la predisposizione al morbo di Crohn e ad altre malattie autoimmuni?
Il morbo di Crohn è una malattia infiammatoria intestinale caratterizzata da un'infiammazione cronica dell'apparato digerente.
Si ritiene che la malattia sia una patologia autoimmune, in cui il sistema immunitario attacca le cellule dell'organismo stesso. Normalmente, le cellule del sistema immunitario riconoscono gli antigeni presenti sulle nostre cellule (autoantigeni) e quelli di organismi innocui (ad esempio i batteri intestinali benefici) e, di conseguenza, non attivano una risposta immunitaria contro queste cellule. Questa capacità di non attaccare le nostre cellule è nota come tolleranza immunologica.
In condizioni autoimmuni come il morbo di Crohn, tuttavia, si verifica una perdita di tolleranza immunologica, che induce il sistema immunitario ad attaccare le cellule che esprimono autoantigeni. I linfociti T citotossici attivati contro questi autoantigeni cercheranno di distruggere tali cellule, mentre i linfociti T helper orchestreranno una risposta infiammatoria e i linfociti B potrebbero produrre anticorpi diretti contro gli autoantigeni (noti come autoanticorpi).

Nel caso specifico del morbo di Crohn, si ritiene che il sistema immunitario attacchi gli autoantigeni presenti nel rivestimento intestinale. Le cellule T prendono di mira anche i batteri intestinali innocui. Entrambi questi processi autoimmuni provocano infiammazione e danni ai tessuti della parete intestinale.
- Varianti del gene ERAP2 e morbo di Crohn
Alcuni studi suggeriscono che la variante «C» (rs2549794) del gene ERAP2, che offre una maggiore protezione dalla peste e da altre infezioni respiratorie, sia associata a un rischio più elevato di sviluppare il morbo di Crohn.
Una meta-analisi del 2010, che ha messo a confronto i genotipi del gene ERAP2 di 6.333 persone affette da morbo di Crohn con quelli di 15.056 soggetti sani di controllo, ha rilevato che la variante «C» era associata a un aumento del 5% del rischio di sviluppare il morbo di Crohn.
A conferma di questo risultato, un recente studio pubblicato in versione preprint ha rilevato che la variante «T» era associata a una riduzione del 14,4% del rischio di sviluppare il morbo di Crohn. Lo stesso studio ha inoltre associato la variante «T» a una riduzione del 5,4% del rischio di diabete di tipo I, un’altra malattia autoimmune.

Scopri il tuo DNA della salute e del benessere
Scopri cosa rivela il tuo DNA sulla tua risposta all'allenamento. Basta con le supposizioni. Inizia ad allenarti in base al tuo DNA. A partire da 279 £.
Risultati disponibili entro 3-4 settimane.


.png)
