Caratteristiche
Caratteristica: riparazione del DNA e longevità (TP53)
Dott. Haran Sivapalan
/
3 gennaio 2022

Cosa sono i geni/le proteine oncosoppressori?
Affinché possiamo crescere, svilupparci e mantenere la normale funzionalità dei tessuti, le nostre cellule devono dividersi e replicarsi.
Prendiamo ad esempio la nostra pelle. Se avete mai pulito una stanza piena di polvere, forse non vi sorprenderà sapere che ogni minuto perdiamo circa 30.000-40.000 cellule cutanee (è risaputo, infatti, che la polvere domestica sia composta in gran parte da cellule cutanee morte). A causa di questo elevato ricambio, le nostre cellule cutanee devono dividersi regolarmente per rimpiazzare quelle perse e mantenere il normale funzionamento della pelle.
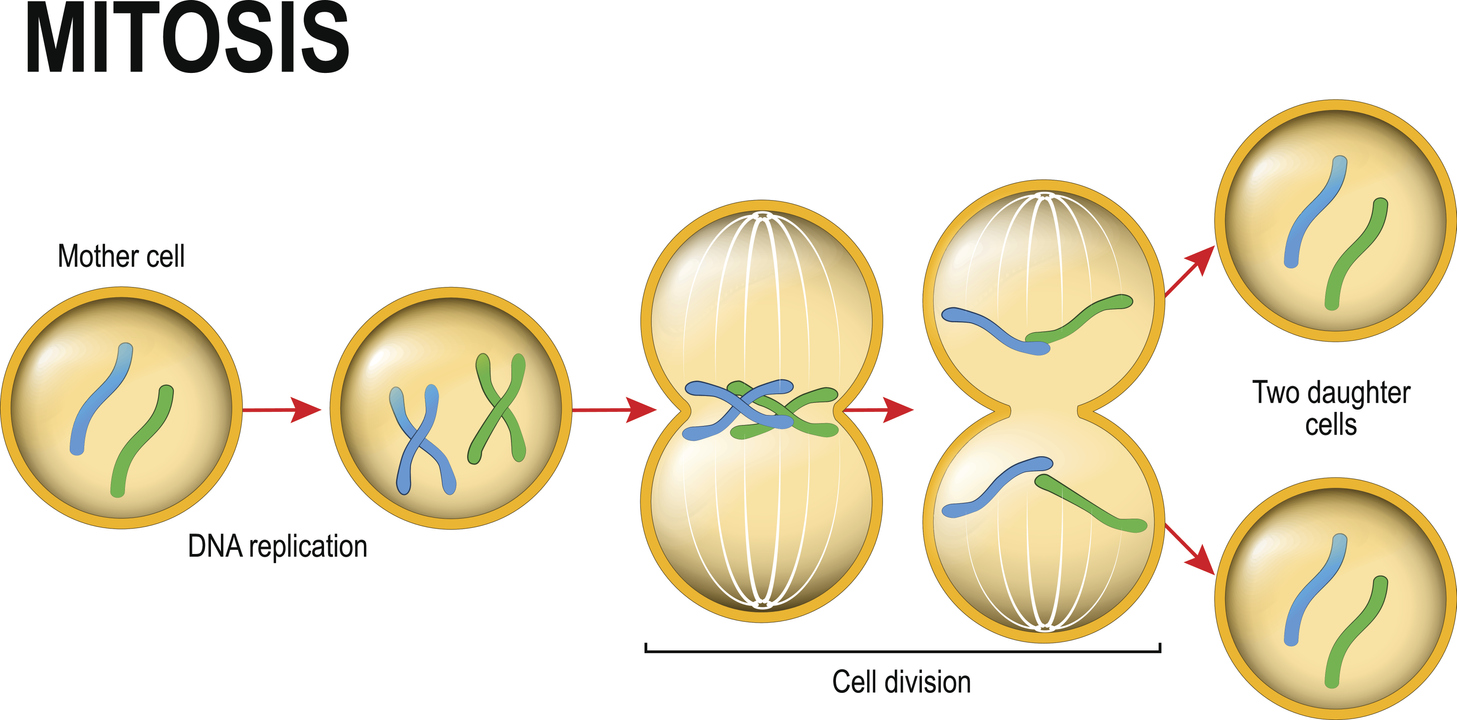
Delle circa 37 trilioni (ovvero 37.000.000.000.000) di cellule presenti nel nostro corpo, circa 2 trilioni si dividono ogni giorno. Questo processo di divisione cellulare (noto come mitosi), tuttavia, deve essere regolato. Se le cellule potessero dividersi in modo incontrollato, ci ritroveremmo con un eccesso di tessuto che comprometterebbe ben presto la nostra salute. Ad esempio, senza controlli sulla divisione cellulare, si ritiene che una persona di 80 anni accumulerebbe 2 tonnellate di midollo osseo e linfonodi e svilupperebbe un intestino lungo 16 km!
Ancora più grave è il fatto che, se un gruppo di cellule dovesse dividersi in modo incontrollato, potrebbe diffondersi e invadere altri organi, compromettendone il funzionamento. Questo è essenzialmente ciò che accade in un tumore maligno, dove una massa anomala di cellule si diffonde in altre parti del corpo.
Un altro motivo per cui è necessario regolare la divisione cellulare è impedire alle cellule danneggiate di moltiplicarsi e di generare future generazioni di cellule danneggiate. Se una cellula subisce un danno al DNA o eredita errori nel proprio codice genetico, tali errori (se non vengono riparati) verranno trasmessi alle cellule figlie al momento della divisione. Se non si interviene, i tessuti e gli organi finirebbero per essere composti in misura sempre maggiore da cellule danneggiate e potrebbero smettere di funzionare correttamente.
Abbiamo spiegato perché è necessario regolare la divisione cellulare, ma come si fa esattamente?
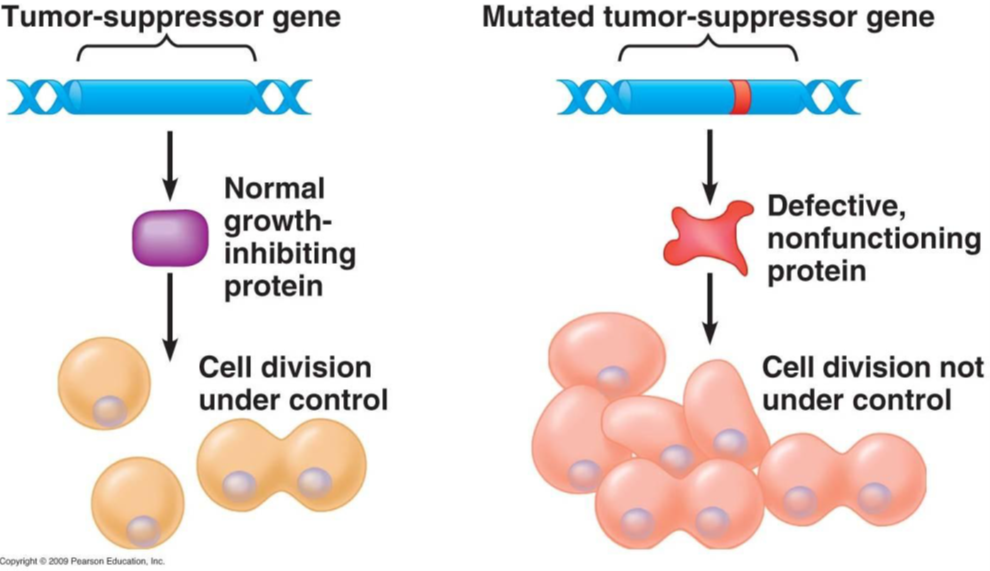
Entrano in gioco i geni oncosoppressori. Si tratta di geni specializzati che, una volta attivati, agiscono come un freno per rallentare o arrestare la divisione cellulare. I geni oncosoppressori codificano proteine, chiamate proteine oncosoppressive, che impediscono alle cellule di dividersi e replicarsi. Si dice che tali proteine fungano da «guardiani» della divisione cellulare.
Le proteine oncosoppressive possono anche riparare il DNA danneggiato (un processo noto come «funzione di riparazione») o indurre le cellule danneggiate a «commettere suicidio cellulare» attraverso un processo di morte cellulare programmata chiamato«apoptosi». Parleremo più approfonditamente dell’apoptosi nella prossima sezione.
Se i geni oncosoppressori vengono inattivati o subiscono mutazioni, tuttavia, potrebbero non essere più in grado di controllare la divisione cellulare. Di conseguenza, le cellule in cui i geni oncosoppressori sono inattivati possono dividersi in modo incontrollato, formando masse cellulari anomale: i tumori.
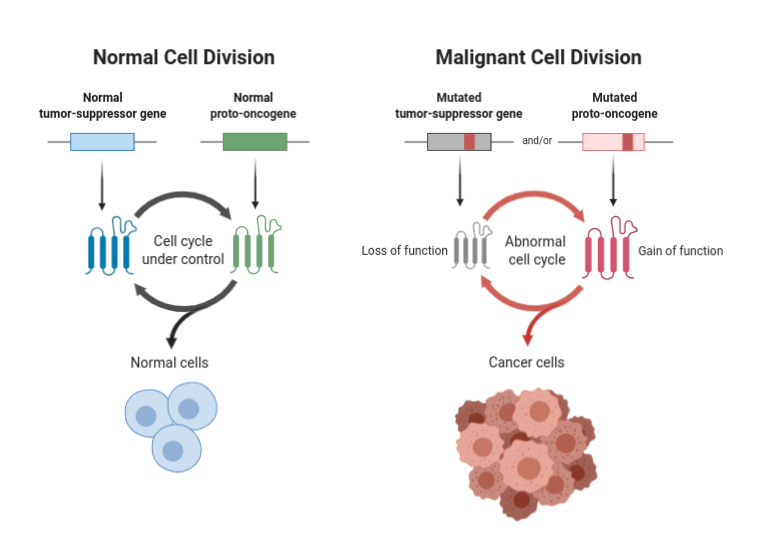
Fonte: BioRender (2021). Geni oncosoppressori e proto-oncogeni. Estratto da https://app.biorender.com/biorender-templates/t-5ed6b0f2cc82d300ae329495-tumor-suppressor-genes-and-proto-oncogenes
È proprio da qui che deriva il termine «gene oncosoppressore». Studi sul retinoblastoma, un raro tumore oculare infantile, hanno rilevato che le cellule tumorali presentavano due copie inattive di un gene chiamato Rb. Ulteriori esperimenti di laboratorio, in cui sono stati inseriti geni Rb normali nelle cellule del retinoblastoma, hanno dimostrato che ciò impediva loro di dividersi in modo incontrollato. La variante normale e attiva del gene Rb stava quindi sopprimendo la formazione dei tumori del retinoblastoma.
Da allora sono stati identificati numerosi altri geni oncosoppressori, tra cui: APC, BRCA1, BRCA2 e il gene oggetto di questa caratteristica, il p53. Tutti questi geni svolgono un ruolo nella regolazione della divisione cellulare, nella prevenzione della crescita cellulare incontrollata e nella riparazione del DNA danneggiato.
Mutazioni rare all'interno di questi geni possono causare o aumentare la predisposizione a vari tipi di tumore. Ad esempio, le mutazioni nel gene APC possono causare una patologia nota come poliposi adenomatosa familiare (FAP), caratterizzata dalla presenza di centinaia o migliaia di piccole escrescenze (polipi) nel colon. Se non trattate, queste possono evolvere in tumore del colon-retto.
In linea di massima, FitnessGenes non riporta le mutazioni genetiche rare che presentano un forte legame con il cancro. Questo perché riteniamo che questo tipo di risultati del test del DNA richieda un'adeguata consulenza genetica e un colloquio con professionisti sanitari qualificati.
A questo proposito, prenderemo in esame solo gli SNP comuni del gene P53 che non presentano un nesso significativo con il rischio di cancro.
PUNTI CHIAVE
- Le cellule dispongono di meccanismi di protezione che impediscono alle cellule danneggiate e mutate di replicarsi e di trasmettere i propri errori.
- Le proteine oncosoppressive sono proteine specializzate che inibiscono la divisione cellulare e proteggono dalla crescita cellulare incontrollata.
- Le proteine oncosoppressive sono codificate dai geni oncosoppressori.
- Le mutazioni nei geni oncosoppressori possono causare una crescita cellulare incontrollata e lo sviluppo di tumori.
- FitnessGenes non analizza le mutazioni fortemente associate al cancro, poiché riteniamo che tali informazioni debbano essere fornite solo nell'ambito di un'adeguata consulenza genetica.
Che cos'è il p53?
Una delle proteine oncosoppressive più studiate è la p53.
È stato comunemente soprannominato il «custode del genoma», poiché contribuisce a riparare il DNA danneggiato e funge da guardiano o filtro per impedire alle cellule con DNA danneggiato o mutato di dividersi.
Il gene p53 viene attivato in risposta a danni al DNA e ad altri tipi di stress cellulare, quali la carenza di ossigeno (ipossia), la privazione di nutrienti e lo stress ossidativo.
Quando viene attivata, la proteina p53 attiva una serie di geni che riparano il DNA danneggiato, rallentano o arrestano la divisione cellulare e avviano altri cambiamenti volti a impedire la crescita cellulare incontrollata e la formazione di tumori. Nel loro insieme, queste risposte protettive al danno al DNA sono note, in modo appropriato, come «risposta al danno al DNA».
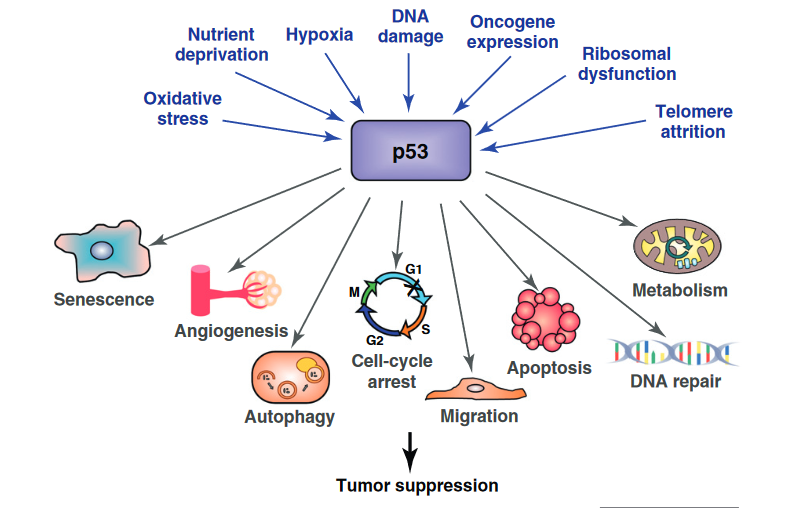
Fonte: Bieging, K. T., & Attardi, L. D. (2012). Analisi delle reti trascrizionali di p53 nella soppressione tumorale. Trends in Cell Biology, 22(2), 97-106.
In particolare, la proteina p53 attiva tre diversi percorsi della nostra risposta al danno al DNA.
- Il gene p53 attiva i meccanismi di riparazione del DNA per riparare le regioni di DNA danneggiate.
- La proteina p53 “blocca” le cellule danneggiate in determinati punti del loro ciclo cellulare per impedire loro di dividersi (arresto del ciclo cellulare).
- Il gene p53 induce le cellule gravemente danneggiate ad autodistruggersi attraverso la morte cellulare programmata (apoptosi).
Si ritiene che la proteina p53 svolga un ruolo fondamentale nel prevenire la crescita cellulare incontrollata e lo sviluppo del cancro, riparando il DNA danneggiato, impedendo alle cellule danneggiate di dividersi e distruggendo quelle irreparabilmente danneggiate attraverso l'apoptosi. Esaminiamo questi tre processi più nel dettaglio.
Riparazione del DNA
Come spiegato nell'articolo dedicato all'ATM e ai danni al DNA, le molecole di DNA presenti nelle nostre cellule possono subire diversi tipi di danni, quali rotture di uno o entrambi i filamenti (rotture a singolo e doppio filamento), legami anomali tra i filamenti, accoppiamenti errati delle basi (le basi sono le «lettere» che compongono la sequenza del DNA) oppure l'inserimento o la delezione di basi.
Se non vengono riparati, questi cambiamenti indesiderati nella struttura e nella sequenza delle molecole di DNA potrebbero portare alla produzione di proteine difettose, interferire con importanti processi cellulari e, in ultima analisi, compromettere il funzionamento delle cellule e dei tessuti.
Fortunatamente, come illustrato nella sezione dedicata al meccanismo ATM e al danno al DNA, le nostre cellule dispongono di vari meccanismi di riparazione in grado di riparare il DNA danneggiato. Ad esempio, disponiamo di diversi enzimi in grado di praticare un'incisione in una molecola di DNA, asportare le basi danneggiate e poi ricomporre la molecola di DNA, proprio come un chirurgo potrebbe aprire e poi sbrigliare una ferita infetta per rimuovere il tessuto necrotico prima di ricucirla.
In risposta al danneggiamento del DNA, i livelli della proteina p53 aumentano rapidamente. La p53 attiva quindi i vari enzimi e le vie di riparazione responsabili del ripristino del DNA danneggiato.
Arresto del ciclo cellulare
- Il ciclo cellulare
Si tratta ovviamente di una semplificazione eccessiva che non vale per tutti, ma si può dire che il ciclo di vita di un essere umano comprenda la nascita come neonato, diversi anni di crescita e sviluppo, la ricerca di un partner e infine la nascita di un nuovo bambino, per poi ripetere il ciclo.
Allo stesso modo, il ciclo vitale di una singola cellula prevede che essa si formi per divisione dalla cellula madre, cresca di dimensioni, replichi il proprio DNA, per poi dividersi (per mitosi) e dare origine a due nuove cellule figlie.
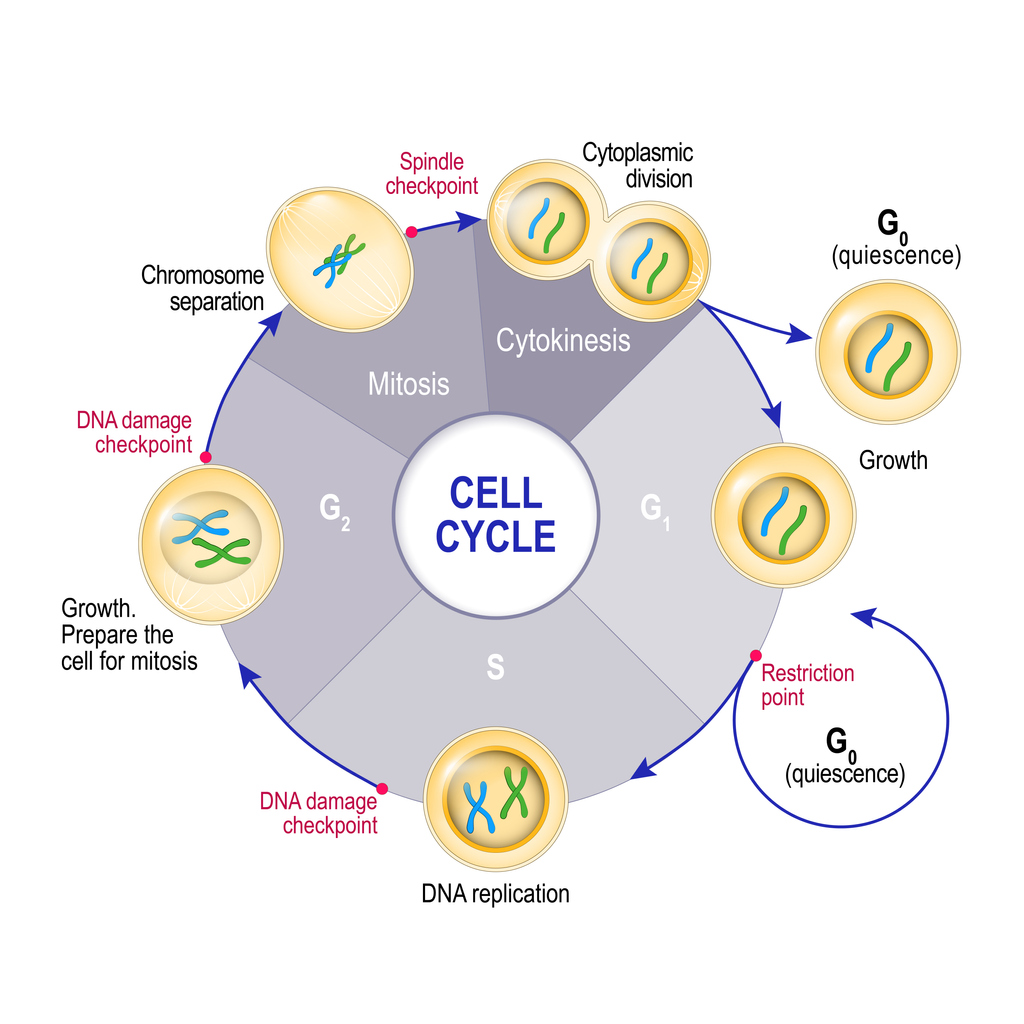
Questo ciclo di crescita e divisione è noto come ciclo cellulare. Il ciclo cellulare può essere suddiviso in 4 fasi distinte:
- G1 (prima fase di intervallo) – una cellula appena formata cresce di dimensioni, accumula sostanze nutritive e sviluppa i propri organelli. Al termine di questa fase, la cellula può “decidere” se uscire dal ciclo ed entrare in uno stato di riposo o “quiescente” (G0), oppure proseguire nella fase successiva del ciclo cellulare (S) e prepararsi a dividersi in nuove cellule figlie.
- S ( fase di sintesi del DNA) – la cellula replica il proprio DNA (che è organizzato in cromosomi) per creare il codice genetico di due nuove cellule figlie.
- G2 ( fase di stallo secondaria) – la cellula continua a crescere e sviluppa gli organelli in preparazione alla divisione mitotica in due cellule figlie.
- M ( fase mitotica) – il DNA e i cromosomi duplicati vengono separati (separazione cromosomica) e il citoplasma della cellula si divide in due (citochinesi), formando due nuove cellule figlie. Il ciclo può quindi ricominciare.
Punti di controllo del ciclo cellulare
Come sottolineato in precedenza, se una cellula danneggiata o mutata potesse completare il ciclo cellulare senza alcun controllo, eventuali errori nel suo DNA verrebbero trasmessi alle nuove cellule figlie durante la divisione. Poiché queste cellule figlie ricominciano a loro volta il proprio ciclo cellulare, tali errori potrebbero proliferare rapidamente, portando all’accumulo di cellule anomale.
Per impedire alle cellule danneggiate di dividersi, il ciclo cellulare prevede diversi punti di controllo integrati che garantiscono che tutto proceda secondo i piani. Si possono paragonare questi punti di controllo alla serie di controlli di sicurezza a cui si è sottoposti quando si prende un volo per un altro Paese (ad esempio: check-in, controllo del bagaglio a mano, gate d’imbarco, controllo passaporti e doganale, ecc.).
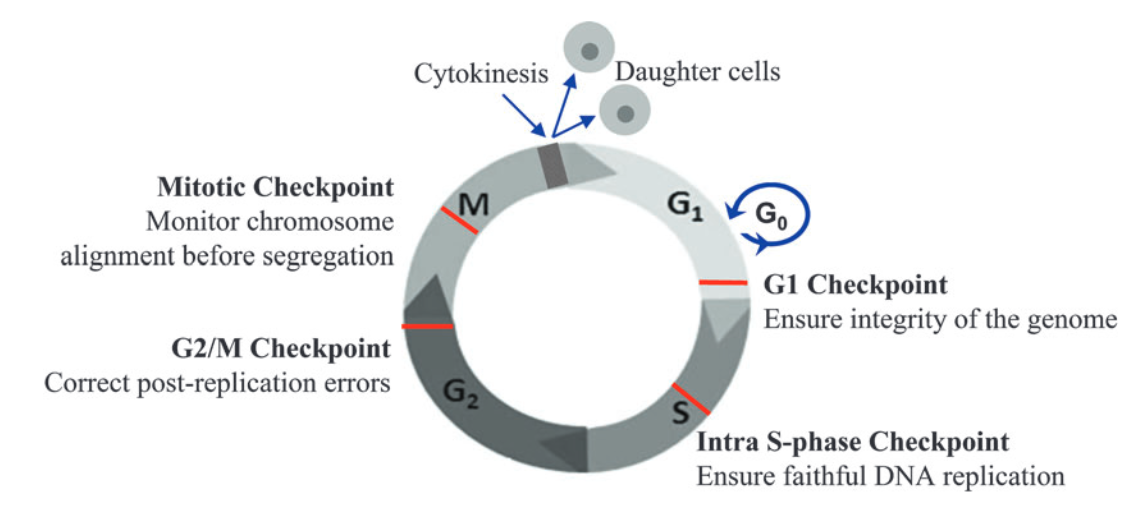
Fonte: Ma W. (2014) Cell Cycle Checkpoint. In: Schwab M. (a cura di) Encyclopedia of Cancer. Springer, Berlino, Heidelberg. https://doi.org/10.1007/978-3-662-46875-3_996
Ci sono 4 fasi fondamentali che una cellula attraversa nel ciclo cellulare:
- Checkpoint G1 – Questo checkpoint si verifica alla fine della fase G1, in corrispondenza della transizione G1/S. Verifica che la cellula sia sufficientemente sviluppata e di dimensioni adeguate per dividersi, che disponga di nutrienti accumulati in quantità sufficiente per la divisione cellulare e, soprattutto, che non vi siano danni al DNA. Una volta che una cellula ottiene il permesso di superare il checkpoint G1, è sostanzialmente destinata a proseguire attraverso il resto del ciclo cellulare e a dividersi. Il checkpoint G1 è quindi cruciale ed è noto come punto di restrizione.
- Punto di controllo intra-S: questo punto di controllo si attiva durante la fase S per verificare la presenza di danni al DNA durante la replicazione.
- Punto di controllo G2/M – questo punto di controllo si verifica alla fine della fase G2, immediatamente prima della fase M. Serve a verificare se il DNA è stato replicato correttamente durante la fase S e se sono presenti danni al DNA. Eventuali errori nelle molecole di DNA in questa fase finiranno nelle due nuove cellule figlie che si formano durante la mitosi, rendendo il punto di controllo G2/M un altro punto di controllo fondamentale.
- Punto di controllo mitotico (del fuso) – questo punto di controllo garantisce che i cromosomi siano correttamente allineati per poter essere distribuiti in due nuove cellule figlie durante la mitosi.
Cosa succede, quindi, se viene rilevato un danno al DNA nei vari punti di controllo del ciclo cellulare?
I due principali punti di controllo regolati dalla proteina p53 sono i punti di controllo G1 e G2/M. Se in uno di questi punti di controllo viene rilevato un danno al DNA, la proteina p53 impedisce alla cellula di proseguire nel resto del ciclo cellulare. Questo fenomeno è noto come arresto del ciclo cellulare.
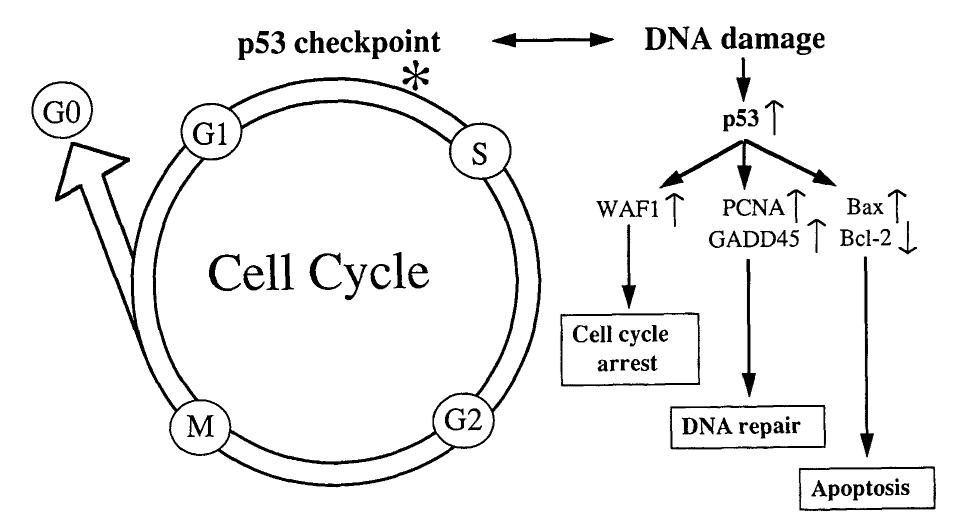
Fonte: Baas, I. O., Offerhaus, G. J. A. e Hruban, R. H. (1997). Interazioni tra il citomegalovirus e il gene oncosoppressore p53 nelle malattie vascolari aterosclerotiche. Clinical Microbiology and Infection, 3(4), 393-395.
Una volta bloccata in questi punti di controllo, la proteina p53 può quindi attivare i meccanismi di riparazione del DNA (descritti in precedenza) per riparare eventuali regioni danneggiate del DNA. Se il DNA danneggiato viene riparato con successo, la cellula può quindi passare alla fase successiva del ciclo cellulare.
In particolare, al punto di controllo G1, le cellule possono essere indotte a uscire dal ciclo cellulare ed entrare nella fase quiescente G0. In questa fase G0, la cellula non si divide, ma rimane in uno “stato di riposo” in cui continua a essere metabolicamente attiva e a funzionare normalmente.
Alcune cellule entrano in questo stato solo temporaneamente e possono rientrare nel ciclo cellulare quando le condizioni lo consentono: questo fenomeno è noto come quiescenza. Al contrario, le cellule danneggiate possono essere indotte a entrare irreversibilmente nella fase G0, risultando permanentemente incapaci di crescere e dividersi. Questo fenomeno è noto come senescenza ed è anch’esso regolato dalla proteina p53. Costringendo le cellule danneggiate a diventare senescenti e incapaci di dividersi, la proteina p53 contribuisce a prevenire la crescita incontrollata di cellule anomale.
In alcuni casi, una cellula può subire un danno al DNA così grave da non poter essere riparato. In questi casi, anziché essere temporaneamente bloccata a un punto di controllo del ciclo cellulare, la proteina p53 ordina alla cellula di autodistruggersi. Questo processo di morte cellulare programmata è noto come apoptosi.
Apoptosi
L'apoptosi, comunemente definita «suicidio cellulare», è un processo di morte cellulare programmata.
Durante l'apoptosi, le cellule si contraggono e sviluppano delle «vescicole» sulla loro superficie, mentre il nucleo contenente il materiale genetico si condensa. La cellula si divide quindi in piccoli frammenti noti come corpi apoptotici, che vengono poi fagocitati dai globuli bianchi (un processo chiamato fagocitosi).
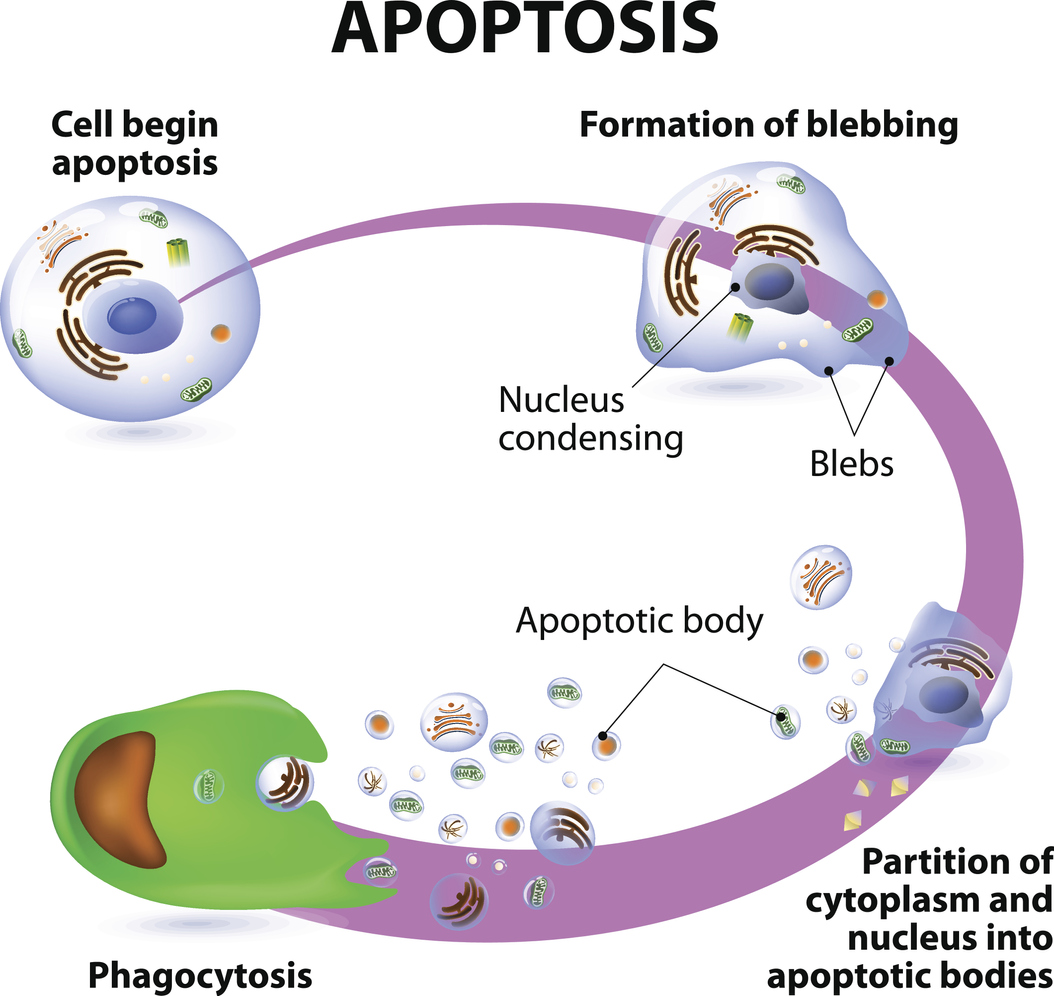
Sebbene l'apoptosi possa sembrare un evento patologico, in realtà si tratta di un processo normale e controllato che viene spesso utilizzato per eliminare le cellule che non sono più necessarie. Le cellule dei feti in fase di sviluppo subiscono l'apoptosi, ad esempio, durante la formazione dei tessuti e degli organi.
L'apoptosi viene utilizzata anche per eliminare le cellule che potrebbero rappresentare una minaccia se lasciate dividersi. Ad esempio, le cellule infettate da un virus sono spesso soggette all'apoptosi per impedire la diffusione dell'infezione in altre parti dell'organismo.
Anche le cellule con gravi danni al DNA vengono distrutte tramite apoptosi. Dopo aver bloccato le cellule danneggiate ai punti di controllo G1 e G2/M, la proteina p53 può indirizzare verso l'apoptosi tutte le cellule che presentano danni al DNA irreparabili. Se queste cellule non venissero eliminate, potrebbero proseguire il ciclo cellulare, dividersi e trasmettere il danno al DNA alle cellule successive, causando l'accumulo di cellule anomale.
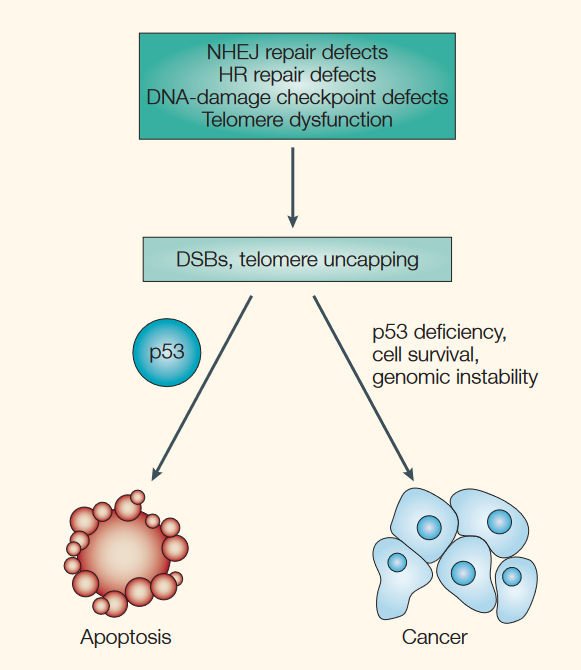
Fonte: Brown, J. M., & Attardi, L. D. (2005). Il ruolo dell'apoptosi nello sviluppo del cancro e nella risposta al trattamento. Nature Reviews Cancer, 5(3), 231-237.
A questo proposito, si osserva spesso che le cellule tumorali presentano una funzione p53 alterata, il che permette loro di eludere l’apoptosi e di dividersi in modo incontrollato. Stimolando l’apoptosi, la proteina p53 contribuisce a prevenire lo sviluppo dei tumori. Analogamente, la chemioterapia e la radioterapia utilizzate nel trattamento del cancro agiscono in parte stimolando le cellule tumorali a subire l’apoptosi.
PUNTI CHIAVE
- La p53 è una delle proteine oncosoppressive più studiate nelle cellule.
- Il gene p53 agisce per inibire la divisione delle cellule danneggiate e impedire una crescita cellulare incontrollata.
- Il gene p53 viene attivato in risposta a danni al DNA e ad altre forme di danno cellulare, come ad esempio la carenza di ossigeno o l'esaurimento delle sostanze nutritive.
- Una volta attivata, la proteina p53 stimola i meccanismi di riparazione del DNA per riparare il DNA danneggiato.
- Il p53 inoltre "blocca" o arresta le cellule danneggiate in determinati punti del loro ciclo cellulare, impedendo loro di replicarsi.
- Le cellule gravemente danneggiate che non possono essere riparate vengono indotte dalla proteina p53 a «suicidarsi» attraverso l'apoptosi, ovvero la morte cellulare programmata.
- Le cellule che sfuggono all'arresto del ciclo cellulare e all'apoptosi possono dividersi in modo incontrollato e diventare cancerose.
Che cos'è il gene TP53?
Il gene p53 è codificato dal nostro gene TP53.
Per usare il gergo biologico, se p53 è una «proteina oncosoppressiva», allora TP53 è il gene oncosoppressivo corrispondente. Il gene TP53 è stato oggetto di numerosi studi in seguito alle osservazioni secondo cui diversi tipi di cellule tumorali presentano mutazioni del gene TP53.
Le cosiddette mutazioni somatiche del gene TP53, che non sono ereditarie e si formano dopo il concepimento, rappresentano una delle alterazioni genetiche più comuni nelle cellule tumorali. Ad esempio, le cellule sane esposte alle radiazioni UV o a sostanze chimiche cancerogene possono subire mutazioni del gene TP53 che le inducono a diventare anomale e a dividersi in modo incontrollato.
Ciò è probabilmente dovuto al fatto che tali mutazioni compromettono la funzione della proteina p53, il che significa che le cellule mutate non vengono riparate, non vengono bloccate ai punti di controllo del ciclo cellulare (e quindi non viene impedita la loro divisione) e non vengono destinate all'autodistruzione tramite apoptosi.
È importante sottolineare ancora una volta che il tratto relativo alla riparazione del DNA e alla longevità non tiene conto delle mutazioni somatiche o delle rare mutazioni ereditarie del gene TP53, che sono strettamente correlate a un malfunzionamento della proteina p53 e al cancro.
Al contrario, prendiamo in esame le varianti comuni del gene TP53 che possono alterare leggermente l'attività della proteina p53, ma che non causano un malfunzionamento della stessa e non sono fortemente associate al cancro.
Varianti del gene TP53
Un comune SNP (polimorfismo a singolo nucleotide) nel gene TP53, denominato rs1042522 o Arg72Pro, provoca una mutazione da G a C nella sequenza del DNA. Ciò crea due diverse varianti del gene TP53 o "alleli": "G" e "C".
L'allele "G" codifica per l'aminoacido arginina nella posizione 72 della proteina p53 ed è quindi chiamato anche allele Arg (Arg72).
Al contrario, l'allele «C» codifica per la prolina nella stessa posizione e può quindi essere indicato come allele Pro (Pro72).
Alcuni studi suggeriscono che gli alleli «G» (Arg) e «C» (Pro) possano alterare l'attività della proteina p53, modificando il modo in cui questa attiva la riparazione del DNA, l'arresto del ciclo cellulare e l'apoptosi in risposta al danno al DNA. Ciò, a sua volta, potrebbe influire sulla durata della vita e sulla longevità.
PUNTI CHIAVE
- Il gene TP53 codifica la proteina oncosoppressore p53.
- Nelle cellule tumorali si osservano mutazioni del gene TP53 che si verificano dopo il concepimento e non sono ereditarie (mutazioni somatiche).
- Il tuo test sulla riparazione del DNA e sulla longevità analizza le varianti comuni ed ereditarie del gene TP53 che non presentano una forte associazione con il cancro.
- Lo SNP rs1042522 (Arg72Pro) dà origine a due varianti/alleli del gene TP53: "C" (Pro) e "G" (Arg).
- È stato dimostrato che le diverse varianti "C" (Pro) e "G" (Arg) alterano l'attività della proteina p53 e influenzano l'efficacia relativa della riparazione del DNA, dell'arresto del ciclo cellulare e dell'apoptosi.
In che modo le varianti comuni del gene TP53 influenzano la funzione della proteina p53?
Come accennato in precedenza, esistono tre meccanismi principali attraverso i quali la proteina p53 reagisce al danno al DNA e impedisce alle cellule danneggiate di replicarsi:
- Riparazione del DNA – attivazione degli enzimi che riparano varie forme di danno al DNA
- Arresto del ciclo cellulare – impedire alla cellula di avanzare nel ciclo cellulare per impedire la divisione cellulare.
- Apoptosi: eliminazione delle cellule con gravi danni al DNA attraverso la morte cellulare programmata.
L'attività relativa di questi tre processi può essere influenzata dalle varianti del gene TP53 che ereditiamo.
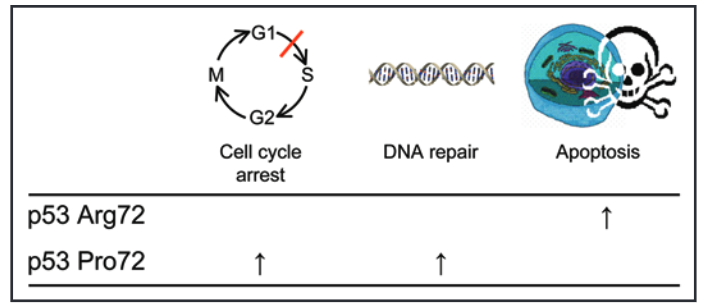
Fonte: Bojesen, S. E., & Nordestgaard, B. G. (2008). Il polimorfismo comune Arg72Pro della linea germinale del gene p53 e l'aumento della longevità nell'uomo. Cell Cycle, 7(2), 158-163.
A questo proposito, alcuni studi hanno dimostrato che l’allele «G» o Arg72 del gene TP53 codifica per una proteina p53 più efficace nel favorire l’apoptosi, ma meno efficiente nella riparazione del DNA e nell’arresto del ciclo cellulare.
Al contrario, l'allele «C» o Pro72 codifica una proteina p53 che risulta relativamente più efficace nella riparazione del DNA e nell'arresto del ciclo cellulare.
È interessante notare che questo allele "C" / Pro72 è stato associato a una maggiore durata della vita e a una maggiore sopravvivenza dopo malattie potenzialmente letali, un effetto che potrebbe essere dovuto a una migliore riparazione del DNA e all'arresto del ciclo cellulare. Inoltre, sebbene l'apoptosi sia indubbiamente cruciale per distruggere le cellule danneggiate e potenzialmente cancerose, è stato ipotizzato che un'apoptosi meno prontamente attivata potrebbe essere benefica, poiché consente alle cellule di rigenerarsi dopo alcune forme di lesione tissutale (ad esempio il danno ischemico) anziché essere eliminate.
PUNTI CHIAVE
- L'allele "C" (Pro) del gene TP53 codifica per una proteina p53 che risulta relativamente più efficace nella riparazione del DNA e nell'arresto del ciclo cellulare.
- L'allele "G" (Arg) codifica per una proteina p53 che è relativamente più efficace nell'attivare l'apoptosi, ovvero la morte cellulare programmata.
- Le varianti del gene TP53 potrebbero influire sulla durata della vita e sulla longevità.
In che modo le varianti del gene TP53 influenzano la durata della vita e la longevità?
Da un'analisi condotta su 9.219 soggetti danesi arruolati nello studio Copenhagen City Heart è emerso che i portatori dell'allele «C» o Pro presentavano un'aspettativa di vita più lunga e una mortalità ridotta dopo una diagnosi di cancro.
Nello studio, ai partecipanti sono stati prelevati campioni di sangue per determinare il loro genotipo TP53 e sono stati poi seguiti per 12 anni. I ricercatori hanno quindi esaminato chi era sopravvissuto nel corso di questo periodo di 12 anni e hanno analizzato se la sopravvivenza fosse correlata alle differenze nei genotipi TP53.
Come illustrato dalla minore pendenza delle linee verde e rossa nel grafico a sinistra riportato di seguito, una percentuale molto maggiore di individui con i genotipi Pro/Pro (CC) e Arg/Pro (GC) è sopravvissuta rispetto a quelli con il genotipo Arg/Arg (GG).
Più precisamente, i soggetti con genotipi Pro/Pro (CC) e Arg/Pro (GC) hanno mostrato una sopravvivenza a 12 anni superiore del 6% e del 3%, rispettivamente, rispetto al genotipo Arg/Arg (GG). Tenendo conto del sesso e dell'età, ciò si traduceva in un rischio di morte per qualsiasi causa inferiore del 18% (CC) e del 12% (GC) rispetto al genotipo GG (Arg/Arg). Analizzando più a fondo i dati, ciò corrispondeva a una sopravvivenza mediana superiore di 3 e 2 anni per i genotipi CC (Pro/Pro) e GC (Arg/Pro).
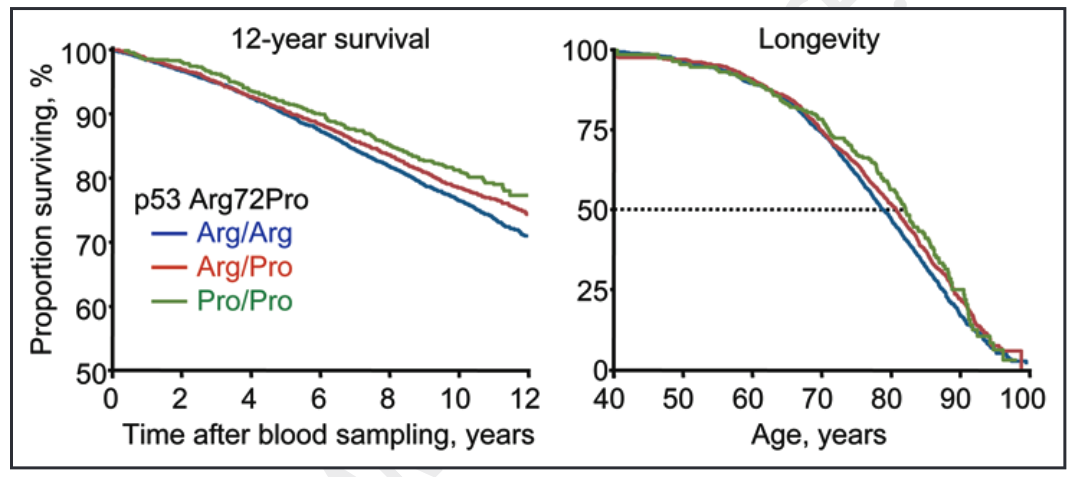
Fonte: Bojesen, S. E., & Nordestgaard, B. G. (2008). Il polimorfismo comune Arg72Pro della linea germinale del gene p53 e l'aumento della longevità nell'uomo. Cell Cycle, 7(2), 158-163.
Allora, perché i portatori dell’allele «C» (Pro) avevano un’aspettativa di vita più lunga?
È interessante notare che i ricercatori non hanno riscontrato alcuna associazione significativa tra il genotipo del gene TP53 e il rischio di sviluppare tumori, malattie cardiovascolari o altre patologie potenzialmente letali.
Lo studio ha invece rilevato che, dopo aver sviluppato un tumore o un'altra malattia potenzialmente letale, i portatori dell'allele «C» (Pro) presentavano una sopravvivenza migliore. A questo proposito, è emerso che i soggetti con genotipi CC (Pro/Pro) e GC (Arg/Pro) presentavano, rispettivamente, una mortalità cumulativa a 5 anni inferiore del 13% e del 9% a seguito di una diagnosi di cancro.
Questo effetto benefico dell'allele "C" / Pro sulla sopravvivenza è evidente nel grafico sottostante, dove si osserva che una percentuale maggiore di individui con genotipo CC (Pro/Pro) (linea verde) e GC (Arg/Pro) (linea rossa) sopravvive nei 5 anni successivi alla diagnosi di cancro.
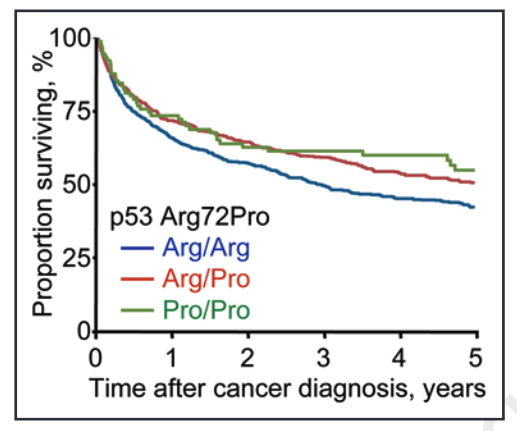
Fonte: Bojesen, S. E., & Nordestgaard, B. G. (2008). Il polimorfismo comune Arg72Pro della linea germinale del gene p53 e l'aumento della longevità nell'uomo. Cell Cycle, 7(2), 158-163.
Lo studio ha inoltre rilevato che i portatori dell'allele "C" (Pro) presentano una maggiore sopravvivenza in seguito a diabete di tipo II, malattie polmonari e infezioni. Un'altra analisi, incentrata sui soggetti anziani dello studio "Leiden 85-plus", ha rilevato che le persone con genotipo CC (Pro/Pro) presentavano un tasso di sopravvivenza superiore del 41%, con una percentuale maggiore di individui con questo genotipo che superavano gli 85 anni di età.
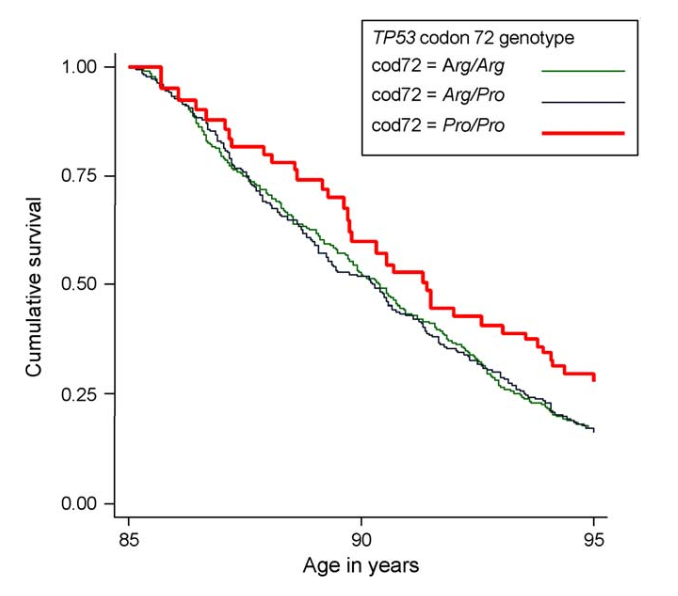
Fonte: van Heemst, D., Mooijaart, S. P., Beekman, M., Schreuder, J., de Craen, A. J., Brandt, B. W., ... & Westendorp, R. G. (2005). La variazione nel gene TP53 umano influisce sulla sopravvivenza in età avanzata e sulla mortalità per cancro. Experimental gerontology, 40(1-2), 11-15.
Le ragioni alla base di questa correlazione tra l'allele «C» (Pro) del gene TP53 e la longevità non sono chiare ed è necessario approfondire gli studi sui meccanismi biologici sottostanti.
Poiché l'allele «C» codifica per una proteina p53 più efficace nell'attivare la riparazione del DNA e l'arresto del ciclo cellulare, è possibile che ciò conferisca una maggiore resistenza alle malattie potenzialmente letali, come il cancro. Analogamente, come accennato in precedenza, è anche possibile che la ridotta attivazione dell'apoptosi nei portatori dell'allele «C» / Pro possa aumentare la sopravvivenza delle cellule in seguito a un danno.
PUNTI CHIAVE
- Alcuni studi hanno associato l'allele "C" (Pro) del gene TP53 a una maggiore durata della vita e a una maggiore longevità.
- L'allele "C" (Pro) è stato inoltre associato a una maggiore sopravvivenza dopo una diagnosi di cancro.
- Questi effetti potrebbero essere dovuti a una riparazione del DNA relativamente più efficace e a un arresto del ciclo cellulare più marcato nei portatori dell'allele «C» (Pro).
- Una maggiore attivazione dell'apoptosi nei portatori dell'allele "G" (Arg) potrebbe compromettere la rigenerazione cellulare in seguito ad alcuni tipi di danno, sebbene ciò non sia stato dimostrato.
In che modo le varianti comuni del gene TP53 influenzano il rischio di cancro?
Poiché la proteina p53 svolge un ruolo fondamentale nella protezione contro la crescita cellulare incontrollata e la formazione di tumori, è lecito supporre che le varianti comuni del gene TP53 influenzino il rischio di cancro.
In linea generale, affinché una cellula diventi cancerosa e si divida in modo incontrollato, devono verificarsi le seguenti condizioni:
- Deve accumulare danni al DNA che non vengono riparati.
- Deve eludere i controlli ai punti di controllo del ciclo cellulare.
- Deve eludere l'apoptosi.
Sulla base di ciò, ci si potrebbe aspettare che l'allele «C» (Pro), associato a una maggiore capacità di riparazione del DNA e all'arresto del ciclo cellulare, conferisca una maggiore protezione contro il cancro rispetto all'allele «G» (Arg).
Al contrario, è plausibile che l’allele «G» (Arg), che potrebbe attivare in modo più efficace l’apoptosi delle cellule precancerose gravemente danneggiate, conferisca una maggiore protezione contro il cancro.
Gli studi condotti finora su vari tipi di tumore presentano un quadro contrastante. Alcuni studi hanno rilevato un'associazione tra l'allele «G» (Arg) e un rischio maggiore di cancro. Ad esempio, una meta-analisi di studi condotti su popolazioni subsahariane ha rilevato che l'allele «G» (Arg) era associato a un rischio maggiore di cancro cervicale.
Al contrario, altri studi hanno associato l’allele «C» (Pro) a un rischio maggiore di cancro. Ad esempio, una meta-analisi del 2020 ha rilevato un rischio maggiore di cancro al seno nelle portatrici dell’allele «C» (Pro).
Diversi altri studi non hanno riscontrato alcun legame tra il genotipo del gene TP53 e il rischio di cancro. Una meta-analisi di studi sul melanoma, un tipo di tumore della pelle, non ha rilevato alcuna differenza significativa nel rischio quando si confrontano i genotipi del gene TP53.
È importante ribadire ancora una volta che le varianti comuni del gene TP53 basate sullo SNP rs1042522 (Arg72Pro) non presentano una correlazione significativa con il cancro. Anche negli studi che riportano associazioni significative tra il genotipo del TP53 e il rischio di cancro, gli odds ratio riportati sono piuttosto modesti, il che suggerisce solo un leggero aumento della suscettibilità.
Possiamo mettere a confronto questo fenomeno con le rare mutazioni ereditarie del gene TP53, non analizzate da FitnessGenes, che possono causare la sindrome di Li-Fraumeni. Queste rare mutazioni provocano un malfunzionamento della proteina p53, determinando una suscettibilità al cancro molto maggiore. Infatti, gli uomini e le donne affetti da sindrome di Li-Fraumeni hanno un rischio di cancro ≥70% e ≥90%, rispettivamente, nel corso della loro vita.
PUNTI CHIAVE
- Gli studi che associano le varianti comuni del gene TP53 al rischio di cancro presentano risultati contrastanti.
- Alcuni studi hanno suggerito che l'allele "G" (Arg) conferisca una maggiore protezione contro vari tipi di tumore.
- Altri studi suggeriscono invece che l'allele "C" (Pro) sia associato a un minor rischio di cancro.
- Diversi studi non rilevano alcuna associazione tra il genotipo del gene TP53 e il rischio di cancro.
- È probabile che gli effetti degli alleli «G» (Arg) e «C» (Pro) – entrambe varianti comuni del gene TP53 – sul rischio di cancro siano modesti.
- Alcune rare mutazioni del gene TP53 possono causare la sindrome di Li-Fraumeni, caratterizzata da un rischio molto elevato di sviluppare un tumore.
- FitnessGenes non analizza le mutazioni associate alla sindrome di Li-Fraumeni.
La tua capacità di riparazione del DNA e il tuo tratto di longevità
Il tuo profilo relativo alla riparazione del DNA e alla longevità prende in esame lo SNP rs1042522 (Arg72Pro) nel gene TP53. In base ai risultati del tuo test del DNA, verrai classificato in uno dei tre gruppi seguenti:
- Ridotta capacità di riparazione del DNA: possiedi due copie dell’allele «G» (Arg), associato a una riparazione del DNA meno efficace e all’arresto del ciclo cellulare, ma anche a un’apoptosi che si attiva più facilmente. Il tuo genotipo (GG) non è associato a una maggiore longevità.
- Leggero aumento della riparazione del DNA: possiedi una copia dell'allele «C» (Pro), associato a una riparazione del DNA e a un arresto del ciclo cellulare più efficaci, nonché a una maggiore longevità.
- Maggiore capacità di riparazione del DNA: possiedi due copie dell’allele «C» (Pro), associato a una riparazione del DNA e a un arresto del ciclo cellulare più efficaci, nonché a una maggiore longevità. Questo gruppo genotipico (CC) è associato alla massima longevità.
Per conoscere il tuo risultato, accedi a truefeed.

Scopri il tuo DNA della salute e del benessere
Scopri cosa rivela il tuo DNA sulla tua risposta all'allenamento. Basta con le supposizioni. Inizia ad allenarti in base al tuo DNA. A partire da 279 £.
Risultati disponibili entro 3-4 settimane.


.png)
